添付文書 【ザノサー点滴静注用1g】16. 薬物動態
- 質問
-
【ザノサー点滴静注用1g】
16. 薬物動態
- 回答
-
16.1 血中濃度
16.1.1 5日間連日投与法
日本人の切除不能又は遠隔転移を有する膵・消化管神経内分泌腫瘍患者15例に本剤500mg/m 2を 5 日間連日点滴静脈内投与したとき、反復投与による薬物動態パラメータに影響はなかった 1)。
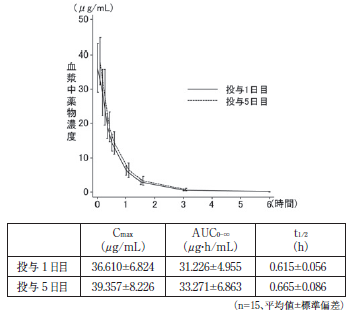
16.1.2 1週間間隔投与法
日本人の切除不能又は遠隔転移を有する膵・消化管神経内分泌腫瘍患者7例に本剤1,000、1,250又は1,500mg/m 2を単回点滴静脈内投与したとき、C max及びAUC 0-∞は投与量に比例して増加した 1)。
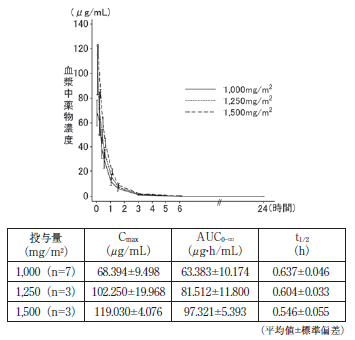
16.2 吸収
記載なし
16.3 分布
16.3.1 血液-脳関門通過性
進行癌患者3例(外国人)に[ 14C]標識ストレプトゾシンをストレプトゾシン総量1,500㎎/m 2(体表面積)で急速静脈内投与 注)した時、全例で脳脊髄液中に[ 14C]が測定され、ストレプトゾシンの代謝物は、血液・脳関門を通過して髄液中に移行するものと考えられる 2)。
16.3.2 髄液への移行性
進行癌患者(外国人)でのストレプトゾシン及びその[ 3H]、[ 14C]標識代謝物の分布に関する検討において、ストレプトゾシン総量1,500mg/m 2(体表面積)を急速静脈内投与 注)した時、脳脊髄液中[ 14C]濃度は3例全例で測定され、投与後 1 時間で血漿中濃度のほぼ1/3、投与後 2 時間では血漿中濃度と同程度であった。一方、脳脊髄液中[ 3H]は投与後 2 時間まで検出されなかった 2)。
注)本剤の用法は「点滴静脈内投与」である。
16.4 代謝
本剤の代謝過程については不明であるが、外国人において、数種類の代謝物が検出されている。これらの代謝物の化学構造は解明されていない 2)。
16.5 排泄
本剤は主に腎臓から排泄される。外国人において、静脈内投与量の約80%が投与後24時間までに、主に代謝物として尿中に排泄された。未変化体としての排泄は投与量の11%であった。本剤もしくは代謝物は、静脈内投与後24時間までに投与量の 5 %程度が呼気中に排泄された。糞中には投与量の 1 %未満が排泄された 2)。
16.6 特定の背景を有する患者
記載なし
16.7 薬物相互作用
記載なし
16.8 その他
記載なし
【文献】
1)Izumi K, et al. : Jpn J Clin Oncol. 2022; 52(7):708-16
2)Adolphe, AB, et al. : Cancer Chemother Rep. 1975; 59(3):547-56
参考になりましたか?
