添付文書 【ラパリムス錠1mg,顆粒0.2%】17. 臨床成績
- 質問
-
【ラパリムス錠1mg,顆粒0.2%】
17. 臨床成績
- 回答
-
17.1 有効性及び安全性に関する試験
〈リンパ脈管筋腫症〉
17.1.1 国際共同第Ⅲ相臨床試験(比較試験)
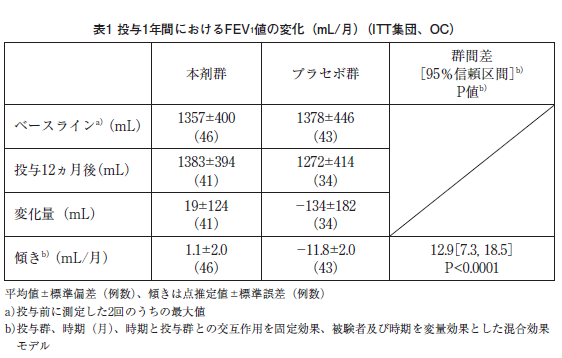
リンパ脈管筋腫症患者89例(全例女性、日本人患者24例を含む)を対象に、プラセボ対照無作為化二重盲検並行群間比較試験(MILES試験)を実施した。錠剤又はプラセボを空腹時又は食後いずれかの条件で経口投与することとし(本剤開始用量は2mg/日)、本剤投与量は、血中トラフ濃度が5~15ng/mLの範囲を維持するよう用量調節した。投与1年間の1秒量(FEV 1)の傾きは表のとおりであり、本剤群とプラセボ群との対比較において、統計学的に有意な差が認められた(P<0.0001)。
副作用は97.8%(45/46例)に発現した。主な副作用は、口内炎63.0%(29/46例)、下痢56.5%(26/46例)、疼痛及びざ瘡43.5%(20/46例)、感染41.3%(19/46例)であった 25)。
17.1.2 国内臨床試験(非盲検試験)
日本人リンパ脈管筋腫症患者63例(全例女性)を対象に、多施設共同非対照非盲検試験(MLSTS試験)を実施した。錠剤を空腹時又は食後いずれかの条件で経口投与することとし(本剤開始用量は2mg/日)、本剤投与量は、血中トラフ濃度が5~15ng/mLの範囲を維持するよう用量調節した。投与2年間のFEV1の傾きは表のとおりであり、傾きの95%信頼区間の下限値は、事前に設定した許容限界を上回り、24ヵ月間安定していた。
副作用は、100%(63/63例)に発現した。主な副作用は、口内炎88.9%(56/63例)、鼻咽頭炎49.2%(31/63例)、上気道の炎症46.0%(29/63例)、発疹41.3%(26/63例)、頭痛39.7%(25/63例)、下痢34.9%(22/63例)、ざ瘡様皮膚炎30.2%(19/63例)であった 8)。(試験終了時)

〈難治性脈管腫瘍及び難治性脈管奇形〉
17.1.3 難治性リンパ管疾患を対象とした第Ⅲ相非盲検試験
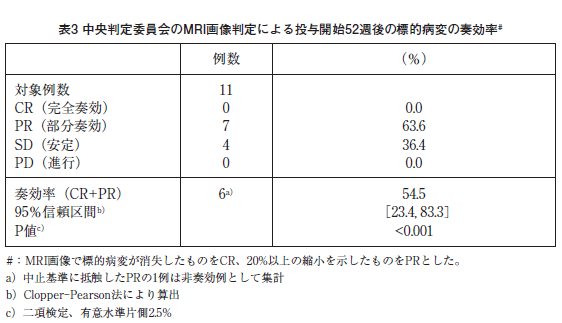
リンパ管腫、リンパ管腫症又はゴーハム病の患者11例を対象に錠剤1日1回1mg(体表面積1.0m 2未満)又は2mg(体表面積1.0m 2以上)を開始用量とし、目標血中トラフ濃度を5~15ng/mLとして52週間投与した。投与52週後の標的病変の奏効率は54.5%で、その95%信頼区間の下限値は事前に設定した閾値(5%)を上回った。
副作用は、100%(11/11例)に発現した。主な副作用は、口内炎81.8%(9/11例)、ざ瘡様皮膚炎72.7%(8/11例)、下痢45.5%(5/11例)、上気道感染36.4%(4/11例)、腹痛、咽頭炎及び発熱各27.3%(3/11例)、気管支炎、皮膚感染、疼痛、咳嗽及び月経過多各18.2%(2/11例)であった 9)。
17.1.4 難治性脈管腫瘍・脈管奇形を対象とした第Ⅲ相非盲検試験
リンパ管腫、リンパ管腫症、カポジ型血管内皮腫、静脈奇形、青色ゴムまり様母斑症候群、混合型脈管奇形又はクリッペル・トレノネー・ウェーバー症候群の患者13例 注1)を対象に、本剤開始用量を1日1回体重30kg以上の場合は錠剤2mg又は顆粒剤1.4㎎、30㎏未満の場合は顆粒剤を月齢に応じて次のとおりとし、血中トラフ濃度を5~15ng/mLとなるよう投与量を適宜調節し52週間経口投与した。
3ヵ月未満:0.02mg/kg/日 注2)
3ヵ月以上6ヵ月未満:0.04mg/kg/日 注2)
6ヵ月以上12ヵ月未満:0.06mg/kg/日
1歳以上:0.08mg/kg/日、ただし1.4mg/日を超えない。
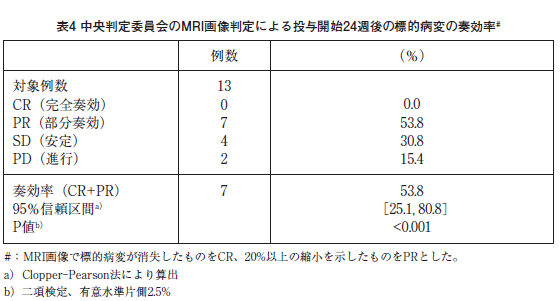
投与24週後の標的病変の奏効率は53.8%で、その95%信頼区間の下限値は事前に設定した閾値(5%)を上回った。
副作用は、100%(13/13例)に発現した。主な副作用は、口内炎76.9%(10/13例)、発熱61.5%(8/13例)、下痢、ざ瘡、好中球数減少各23.1%(3/13例)であった 10)。
注1)ゴーハム病及び房状血管腫も試験の対象とされたが、登録なし注2)登録なし
【文献】
8)社内資料:MLSTS試験 研究総括報告書(2014年7月4日承認、申請資料概要2.7.6.1)
9)社内資料:NPC-12T-LM試験 治験総括報告書(2021年9月27日承認、申請資料概要2.7.6.1)
10)社内資料:NPC-12T-CVA試験 治験総括報告書(2024年1月18日承認、申請資料概要2.7.6.2)
25)McCormack FX, et al. : N Engl J Med. 2011 ; 364(17): 1595-606
参考になりましたか?
