添付文書 【ノベルジン錠25mg・50mg,顆粒5%】16. 薬物動態
- 質問
-
【ノベルジン錠25mg・50mg,顆粒5%】
16. 薬物動態
- 回答
-
16.1 血中濃度
16.1.1 単回投与
ウィルソン病患者23例にノベルジンカプセルを単回投与したときの薬物動態パラメータ(服薬前と服薬後との差に基づく値)及び平均血清中亜鉛濃度(実測値)の推移は以下のとおりであった 8)。
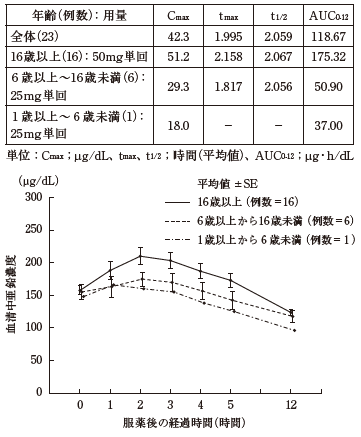
16.1.2 生物学的同等性試験
健康成人男性30例にノベルジン顆粒5%及びノベルジン錠50mg(いずれも亜鉛として50mg)をクロスオーバー法により絶食時に単回経口投与したときの平均血清中亜鉛濃度(服用後の濃度から服用前の濃度を差し引いた濃度)の推移及び薬物動態パラメータ(AUC 0-24及びC max)は以下のとおりであった。AUC 0-24及びC maxの対数の平均値の差について90%信頼区間はlog(0.80)~log(1.25)の範囲内であったことから、生物学的に同等であることが確認された 9)。
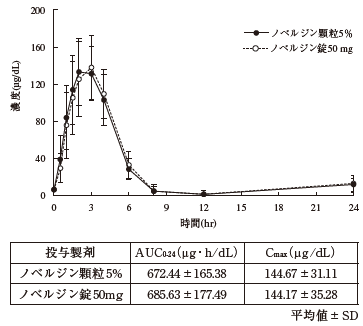
16.2 吸収
記載なし
16.3 分布
記載なし
16.4 代謝
記載なし
16.5 排泄
ウィルソン病患者35例にノベルジンカプセルを投与したときの24時間尿中亜鉛排泄量は以下のとおりであった 8)。
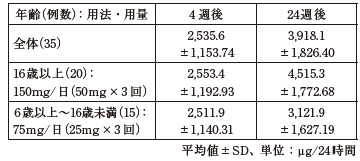
ウィルソン病患者37例にノベルジンカプセルを投与したときのスポット尿中亜鉛排泄量は以下のとおりであった 8)。
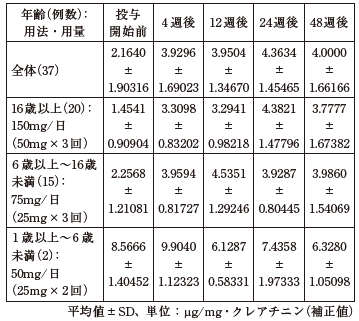
16.6 特定の背景を有する患者
記載なし
16.7 薬物相互作用
記載なし
16.8 その他
記載なし
【文献】
8)社内資料:ウィルソン病に対する国内第Ⅲ相試験(2008年1月25日承認、申請資料概要2.7.6(10))
9)社内資料:錠剤と顆粒剤の生物学的同等性試験(2021年1月22日承認、申請資料概要2.7.6.1)
参考になりましたか?
